Офатумумаб (OMB157) вызывает сильное и быстрое снижение уровней циркулирующих иммунных клеток у людей с рецидивирующими формами рассеянного склероза (РС), эффективно помогая остановить активность болезни, согласно новым данным исследования фазы 2 APLIOS.
Было также обнаружено, что этот препарат более эффективен, чем Aubagio (терифлуномид), в устранении всех признаков активности РС в последующем анализе двух испытаний ASCLEPIOS фазы 3.
Эти новые результаты были недавно представлены практически во время 6- го Конгресса Европейской Академии Неврологии (EAN) и опубликованы в Европейском Журнале Неврологии .
Они также поддерживают атумумаб, находящийся на рассмотрении регулирующих органов в США, решение которого ожидается в июне, в качестве потенциального варианта лечения рецидивирующих форм РС.
Офатумумаб, совместно разработанный Genmab и Novartis, является полностью человеческим антителом, которое специфически нацелено и блокирует активность CD20, белкового рецептора, обнаруженного на поверхности иммунных B-клеток. Считается, что эти иммунные клетки управляют разрушительными иммунными реакциями против миелина — жирового вещества, которое оборачивается вокруг нервных волокон для обеспечения правильного общения с нервными клетками — наблюдается у пациентов с РС.
Ожидается, что блокируя CD20, офатумумаб снизит количество циркулирующих В-клеток и, возможно, ограничит их взаимодействие с другими иммунными клетками, которые являются ключевыми в прогрессировании РС.
Запросы на его одобрение поступают как к Управлению по контролю за продуктами и лекарствами США (FDA), так и к Европейскому агентству по лекарственным средствам (EMA). Решение FDA может быть объявлено в ближайшие недели, а решение EMA ожидается в следующем году.
В случае одобрения офатумумаб станет первой B-клеточной терапией, которую пациенты смогут проводить дома с помощью автоинъекционной ручки SensoReady.
Во время Конгресса EAN Novartis представила данные нового анализа APLIOS ( NCT03560739 ), глобального 12-недельного открытого исследования фазы 2, в котором изучались фармакологические свойства офтумумаба при введении двумя различными устройствами: предварительно заполненный шприц и SensoReady. ручка.
Предыдущие результаты APLIOS показали, что как подкожные (под кожей) устройства доставки оказывали одинаковое воздействие на B-клетки пациентов, так и разумную безопасность.
Новые данные, представленные в плакате « Влияние подкожного офатумумаба на подгруппы лимфоцитов у пациентов с СРК: анализ из исследования APLIOS » (примечание: необходима регистрация EAN для доступа к рефератам и плакатам), подробные выводы о 284 взрослых с рецидивирующими ремиттирующий рассеянный склероз ( RRMS ) или активный вторичный прогрессирующий рассеянный склероз ( SPMS ), которые участвовали в испытании.
Результаты показали, что офатумамаб, вводимый подкожно в дозе 20 мг один раз в месяц, быстро снижал уровни CD20-позитивных В- и Т-клеток. Эти быстрые и устойчивые сокращения были очевидны в нескольких подгруппах иммунных клеток, включая память и наивные В-клетки, а также высокоактивные Т-клетки-киллеры.
В В-клетках значительное снижение стало очевидным к 14 дню и поддерживалось до 84 дня (около 12 недель). Снижение уровня Т-клеток стало очевидным раньше (дни 4–7) и немного возросло на 84 день.
В устной презентации « Раннее влияние офатумумаба на количество В-клеток и активность МРТ у пациентов с рецидивом рассеянного склероза: результаты исследования APLIOS » исследователи представили дополнительные данные из APLIOS, показывающие, что офатумумаб снизил среднее количество поражений МС — с 1,5 на исходном уровне (начало исследования) до 0,1 к 12 неделе и увеличило процент пациентов, которые оставались без повреждений в течение всего исследования — с 64,2% в начале исследования до 94,1% к 12 неделе.
Novartis также представила данные, полученные в результате последующего анализа двух испытаний фазы 3 — ASCLEPIOS I ( NCT02792218 ) и ASCLEPIOS II ( NCT02792231 ), — сфокусированных на оценке шансов пациентов с RRMS или SPMS, использующих офумумаб, для достижения состояния без заболевания.
Результаты этого анализа, основанные на данных, охватывающих 1882 пациента, были представлены в постере « Офатумумаб против терифлуномида при рецидивирующем рассеянном склерозе: анализ отсутствия доказательств активности заболевания (NEDA-3) из испытаний ASCLEPIOS I и II ».
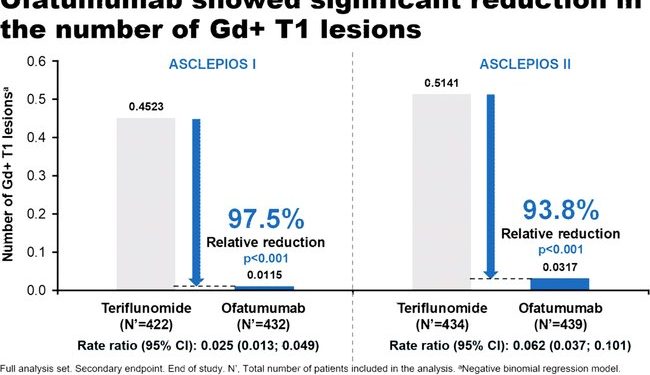
Предыдущие данные ASCLEPIOS показали, что офатумумаб снижал частоту рецидивов и активные поражения мозга у людей с рецидивирующим РС
Новые данные, представленные в EAN, показали, что по сравнению с Aubagio , одобренным препаратом для лечения РС от Sanofi , офатумумаб увеличивал вероятность появления у пациента состояния без заболевания на основе NEDA-3 (нет признаков активности болезни) — определяемого как отсутствие рецидивов, нет шестимесячное ухудшение подтвержденной инвалидности и отсутствие новых или активных поражений РС.
В течение первого года лечения почти половина (47,2%) пациентов, получавших офатумумаб — и четвертый (24,5%) из числа получавших Аубагио — получали NEDA-3. На втором году доля пациентов, получавших офатумамаб, достигших безрецидивного состояния, была почти в два раза выше, чем в группе Aubagio — 87,8% с офатумумабом против 48,2% с Aubagio.
«Отсутствие доказательств активности заболевания широко признано в качестве важной цели лечения для лечения рассеянного склероза. Эти данные свидетельствуют о том, что прекращение новой активности болезни возможно при целенаправленной B-клеточной терапии », — сказал в пресс-релизе Людвиг Каппос, доктор медицинских наук, старший автор исследования .
В другой устной презентации « Влияние офатумумаба на истощение В-клеток и результаты эффективности: анализ подгруппы из объединенных испытаний фазы ASCLEPIOS I и II », исследователи представили дополнительные результаты анализа подгруппы объединенных данных из обоих испытаний ASCLEPIOS.
По сравнению с Aubagio, офатумумаб приводил к более сильному снижению количества B-клеток, независимо от массы тела пациента. Кроме того, офатумумаб продемонстрировал большую эффективность, чем Аубагио, в отношении уменьшения ухудшения инвалидности и числа рецидивов рассеянного склероза, которые пациенты испытывали в течение года.
«Эти результаты вселяют надежду и подтверждают нашу уверенность в том, что в случае одобрения офатумумаб может значительно улучшить жизнь людей с СРК (рецидивирующим РС)», — сказал Кришнан Раманатан, глава Глобальной программы Neuroscience в Novartis.
В ожидании решения FDA относительно потенциального одобрения Офатумумаб в США, компания готовит запросы для его одобрения регулирующими органами в других местах.