Страны во всем мире подтвердили ошеломляющее количество случаев COVID-19, и теперь ясно, что ни одна страна не застрахована от инфекции SARS-CoV-2. Страны с ограниченными ресурсами и более слабыми системами здравоохранения борются с собственными эпидемиями и сейчас находятся в более неопределенной ситуации с этой быстро распространяющейся инфекцией. Передовые медицинские работники умирают от инфекции, пытаясь спасти жизни. Существует срочность разработки методов лечения COVID-19, однако клинические данные об эффективности потенциальных лекарственных препаратов ограничены. Страны во всем мире ввели приказ оставаться дома, чтобы «сгладить кривую» и ослабить давление на систему здравоохранения, но неясно, как это будет развиваться после восстановления экономики. Известно, что трегалоза, природный дисахарид глюкозы, нарушает вирусную функцию через систему аутофагии.
Вступление
Пандемия коронавируса 2019 года (COVID-19), вызванная тяжелым острым респираторным синдромом, вызванным коронавирусом 2 (SARS-CoV-2), быстро распространилась по всему миру. По состоянию на 5 июня 2020 года Всемирная организация здравоохранения (ВОЗ) подтвердила 6 515 796 случаев заболевания и сообщила о 387 298 случаях смерти во всем мире из-за COVID-19. Доступные в настоящее время методы лечения направлены на контроль симптомов, обеспечение перфузии тканей и предотвращение синдрома полиорганной недостаточности. Это достигается за счет использования кислородной терапии, искусственной вентиляции легких в случаях дыхательной недостаточности и гемодинамической поддержки для лечения септического шока ( 1).). К сожалению, передовые системы здравоохранения изо всех сил пытаются справиться с наплывом пациентов с COVID-19, нуждающихся в лечении и госпитализации. Все большую озабоченность вызывает пагубное воздействие этого вируса на страны с более слабыми системами здравоохранения и уязвимыми группами населения. В настоящее время не существует препарата, одобренного Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), который мог бы эффективно контролировать инфекцию и передачу SARS-CoV-2. Этот обзор призван предложить трегалозу в качестве перспективного профилактического средства для сдерживания COVID-19.
Трегалоза (α, α-трегалоза), встречающийся в природе сахар, представляет собой невосстанавливающий дисахарид с двумя молекулами глюкозы, который действует как источник энергии для многих организмов. Трегалоза присутствует в различных организмах, таких как растения, водоросли, грибы, дрожжи, бактерии, насекомые и другие беспозвоночные. В 2000 году FDA США присвоило трегалозе статус, общепризнанный как безопасный (GRAS) ( 2 ). Из-за своего защитного действия против замерзания и обезвоживания трегалоза стала привлекательным ингредиентом в продуктах питания, медицинских и фармацевтических продуктах ( 2). Оптимизированный процесс производства трегалозы делает его доступным и доступным. Хотя люди не могут синтезировать трегалозу, тонкий кишечник может гидролизовать трегалозу до двух молекул D-глюкозы с помощью специфического фермента трегалозы. Поскольку гидролизирующая активность треалазы обычно низкая, она вызывает лишь незначительное повышение уровня глюкозы в крови и инсулина ( 3 , 4 ). Напротив, сахароза, дисахарид, состоящий из глюкозы и фруктозы, сразу же увеличивает уровень глюкозы в крови и инсулина после перорального приема ( 5). С другой стороны, негидролизованная трегалоза может быстро всасываться в кровоток после перорального введения мышам, крысам и макакам, пик которого достигается через ~ 15 минут — 1 час после введения дозы и продолжает обнаруживаться у макак до 12 часов после введения. доза ( 6 , 7 ). Фармакокинетические данные о приматах, кроме человека, являются многообещающим стимулом для реакции человека на трегалозу. У людей ежедневное потребление 10 г трегалозы в день в течение 12 недель улучшало толерантность к глюкозе, уменьшало прогрессирование инсулинорезистентности и снижало систолическое артериальное давление. Следовательно, трегалоза может вызывать системные преимущества, которые не связаны с повышением уровня глюкозы и резистентностью к инсулину ( 8). В целом эти исследования подтверждают осуществимость и безопасность лечения трегалозой для предотвращения инфекции и передачи SARS-CoV-2.
С 1925 года было проведено несколько исследований, направленных на изучение химических и биологических свойств трегалозы. Трегалоза получила внимание благодаря своим защитным свойствам при нейродегенеративных и метаболических заболеваниях ( 9 — 12 ). Считалось, что защитное действие трегалозы связано с ее химическими свойствами шаперона ( 13 ). Однако в 2007 году трегалоза была идентифицирована как индуктор аутофагии ( 14 ). Аутофагия, высококонсервативный процесс внутриклеточной деградации, регулируется основной контрольной комплексной мишенью млекопитающих — рапамицином (mTOR) ( 15 , 16 ). Интересно, что трегалоза вызывает аутофагию независимо от mTOR ( 14). В культурах клеток млекопитающих обработка трегалозой может повысить клиренс денатурированного хантингтина и денатурированного α-синуклеина, обоих субстратов аутофагии, связанных с болезнями Хантингтона и Паркинсона, соответственно ( 14 ). Эффекты трегалозы зависят от накопления ассоциированного с микротрубочками белка 1A / 1B-легкая цепь 3 (LC3) II, который необходим для образования аутофагосом из связанных с аутофагией 5 (ATG5) фагофоров, заякоренных белковым комплексом ( 14 ). Однако они не зависят от ингибирования mTOR, поскольку трегалоза не снижает уровни фосфорилирования в определенных сайтах на субстратах mTOR, которые снижаются ингибитором mTOR рапамицином ( 14). Позже было установлено, что фактор транскрипции EB (TFEB) является первичным регулятором лизосомного биогенеза, поскольку он индуцирует экспрессию нескольких важных генов этого феномена ( 17 ). Когда трегалоза стала индуктором аутофагии, некоторые исследовательские группы были вынуждены использовать трегалозу, чтобы продемонстрировать роль TFEB. Было обнаружено, что трегалоза снижает активность AKT (протеинкиназы B), которая фосфорилирует TFEB (S467A), тем самым обеспечивая транслокацию TFEB в ядро независимо от ингибитора TFEB, mTOR ( 18 ). Кроме того, трегалоза может активировать TFEB и впоследствии способствовать перекрестной презентации ( 18 , 19 ).
При материнском диабете подавленная аутофагия в развивающихся клетках нейроэпителия приводит к дефектам нервной трубки (NTD) у развивающегося плода ( 20 ). Введение трегалозы восстановило этот дефект аутофагии и предотвратило индуцированные гипергликемией NTD ( 21 ). В другом исследовании in vitro трегалоза способствовала образованию аутофагосом LC3 в культивируемых клетках с высоким содержанием глюкозы, более высокому клиренсу убиквитин-связывающего белка p62, дифференцировке нервных стволовых клеток, митофагии и ретикулофагии ( 22).). Синдром Санфилиппо или мукополисахаридоз (МПС) типа III представляет собой нейродегенеративное лизосомное нарушение накопления. Модель MSP III на мышах, обработанная трегалозой, показала неврологические улучшения, связанные с клиренсом аутофагических вакуолей в нейрональных и глиальных клетках, а также с активацией транскрипционной сети TFEB ( 23 ). В модели ремоделирования сердца при инфаркте миокарда использование трегалозы привело к улучшению результатов у мышей дикого типа ( 24 ). С другой стороны, введение трегалозы мышам с генетическим дефицитом Беклина-1, важного белка в регуляции аутофагии, не имело защиты ( 24). Трегалоза также увеличивала клиренс LC3 и p62. Вместе с тем, эти результаты подтвердили, что аутофагия, вызванная трегалозой, вызывает кардиозащитные эффекты ( 24 ). Трегалозы введение также ингибируется и затухает с высоким содержанием жиров индуцированного атеросклероза у мышей и кроликов, соответственно ( 25 — 27 ). Университет медицинских наук Мешхеда в настоящее время спонсирует интервенционное клиническое исследование для проверки положительных эффектов внутривенного введения трегалозы (15 г в неделю в течение 12 недель) в качестве противовоспалительного средства против сосудистого воспаления и атеросклероза ( ClinicalTrials.gov, NCT 03700424). Пациенты с заболеванием периферических артерий (ЗПА) связаны с сосудистыми осложнениями и повышенной активацией тромбоцитов. Снижение окисления глюкозы, окислительный стресс и аутофагия — факторы, которые способствуют снижению кровотока у пациентов с ЗПА ( 28 ). В настоящее время проводится клиническое исследование влияния трегалозы на функцию эндотелия, окислительный стресс, функцию тромбоцитов и аутофагию у пациентов с ЗПА ( ClinicalTrials.gov , NCT 04061070).
В контексте инфекционных заболеваний индукция аутофагии имеет решающее значение для развития как врожденного, так и адаптивного иммунного ответа. Хотя некоторые микроорганизмы могут избегать аутофагии и даже использовать ее в качестве стратегии выживания и размножения, аутофагия является эффективным способом борьбы с большинством внутриклеточных инфекций ( 29 ). Вирус иммунодефицита человека (ВИЧ), патоген, известный своей способностью уклоняться от иммунных ответов, также известен своими эффектами в потоке аутофагии ( 30 ). ВИЧ увеличивает количество аутофагосом и нарушает созревание аутофагосом, тем самым блокируя слияние аутофагосом и лизосом ( 31 ). Несмотря на то, что CD4 +Т-лимфоциты являются преобладающей мишенью для ВИЧ-инфекции, именно ВИЧ-инфицированные клетки врожденного иммунитета делают организмы очень чувствительными к условно-патогенным микроорганизмам, таким как непатогенные микобактерии ( 32 ). Хотя ингибирование аутофагии 3MA или миРНК Beclin-1 снижает продукцию вируса ВИЧ в линии клеток Jurkat ( 31 ), недавнее исследование показало, что трегалоза может восстанавливать аутофагию, нарушенную ВИЧ-инфекцией, в мононуклеарных клетках периферической крови (PBMC) in vitro ( Таблица 1 ) ( 32 ). Кроме того, после лечения трегалозой снижалась нагрузка ВИЧ в PBMC от ВИЧ-инфицированных пациентов ( 32). Противовирусное действие трегалозы на другие вирусы, связанные с заболеванием, такие как цитомегаловирус человека (HCMV) и вирус ветряной оспы (VZV), было продемонстрировано in vitro ( таблица 1 ). Его механизм действия заключается в его способности значительно вызывать аутофагию. Трегалоза подавляла экспрессию вирусного гена HCMV и распространение вируса во многих типах клеток ( 34 ). Как до, так и после лечения трегалозой уменьшалась репликация HCMV и VZV ( 35). Интересно, что Кларк и др. (2018) сообщили о клетках, инфицированных HCMV, о том, что трегалоза изменяет морфологию вирионов внутри мультивезикулярных тел (MVB) и перенаправляет трафик созревания вирусных вакуолей за счет подавления Ras-подобной GTPase 11 (Rab11), белка, участвующего в контроле эндосомного транспорта ( Рисунок 1 ) ( 33 ). В первичных кортикальных культурах мышей, инфицированных вирусом Западного Нила (WNV), трегалоза индуцировала устойчивую активацию аутофагии, о чем свидетельствует увеличение экспрессии белка LC3-II; однако активация аутофагии не оказала значительного влияния на рост ВЗН ( 37 ) ( Таблица 1). Подобная активация аутофагии наблюдалась в эпителиальных клетках первичных дыхательных путей человека, обработанных трегалозой, но индукция аутофагии нарушала противовирусную функцию против инфекции риновируса человека (ВСР) ( 36 ) ( Таблица 1 ).ТАБЛИЦА 1
Таблица 1 . Резюме противовирусных эффектов трегалозы.ФИГУРА 1
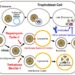
фигура 1. Репликация SARS-CoV2 и ингибирование трегалозой. SARS-CoV-2 получает доступ через слияние мембран, связывая ангиотензин-превращающий фермент 2 (ACE2) в клетке-мишени. Затем вирус интернализуется и транспортируется через эндосомные компартменты. Вирусный геном высвобождается и используется рибосомой хозяина для синтеза вирусной РНК-полимеразы, таким образом реплицируя субгеномы вирусной РНК. Вирусные структурные белки синтезируются и закрепляются в эндоплазматическом ретикулуме (ER). Как только вирион собирается в промежуточном компартменте ER-Golgi (ERGIC) и переносится в аутофагосому, он может высвобождаться из амфисомы путем экзоцитоза. Неструктурный белок 6 (nsp6) и nsp3 коронавируса способствуют образованию аутофагосом, но предотвращают слияние аутофагосом и лизосом. (1) Трегалоза может способствовать слиянию амфисомы и лизосомы для деградации вириона после переноса вирусных двойных мембранных везикул. (2) Трегалоза может также активировать фактор транскрипции EB (TFEB) и способствовать биогенезу лизосом.
Бета-коронавирусы, коронавирус тяжелого острого респираторного синдрома (SARS-CoV) и коронавирус ближневосточного респираторного синдрома (MERS-CoV) кодируют вирусные белки, которые нарушают слияние аутофагосомы и лизосомы, такие как мембраносвязанная папаин-подобная протеаза (PLp- TM) ( 38 ). Кроме того, коронавирусы реплицируются в LC3-опосредованных аутофагосомоподобных двойных мембранных везикулах ATG7-независимым образом ( 39 , 40 ). Поскольку различные вирусы захватывают механизмы аутофагии в пользу репликации вирусов и созревания вирионов, регулирование клеточной аутофагии с помощью модуляторов аутофагии, таких как хлорохин (CQ) или трегалоза, имеет большое значение в лечении вирусных заболеваний ( 41).). В связи с этим коронавирусы экспрессируют неструктурный белок 6 (nsp6) и nsp3, которые способствуют образованию аутофагосом, но предотвращают слияние аутофагосом и лизосом, что указывает на то, что индукция потока аутофагии трегалозой может быть полезной для потенциального сдерживания COVID-19 ( Рисунок 1 ) ( 38 , 42 ). Ангиотензин-превращающий фермент 2 (ACE2) играет важную роль в качестве рецептора SARS-CoVs, опосредующего проникновение вируса через эндоцитоз ( рис. 1 ) ( 43 ). Следует отметить, что недавно описанный эндоцитоз, связанный с LC3 (LANDO), который возникает при конъюгации LC3 с Rab5 + клатрин +эндосомы, содержащие β-амилоид, являются еще одним недавно зарегистрированным важным механизмом очистки экзогенных антигенов в микроглиальных клетках ( 44 ). LANDO может быть еще одной недооцененной LC3-везикулой с потенциалом коронавирусной репликации, что может объяснить LC3-зависимую и ATG7-независимую коронавирусную репликацию, наблюдаемую ранее. Однако дихотомия заключается в том, что и LC3-фагосома, и LC3-эндосома представляют собой везикулы с одной мембраной, в то время как репликация коронавируса может происходить в пузырьках с двойной мембраной ( 40 ). Пока что неизвестно влияние трегалозы на LANDO, но очевидно, что трегалоза проявляет зависимую от аутофагии противовирусную активность против различных типов вирусов.
COVID-19 Терапевтические стратегии, разработки и проблемы
Основными стратегиями замедления распространения COVID-19 и, тем самым, снижения жестких требований к здравоохранению, были изоляция инфицированных в их семье и поощрение социального дистанцирования ( 45 , 46 ). Однако в свете постоянно увеличивающегося числа случаев «домогательства» — это мера, которой придерживаются многие страны, чтобы сдержать распространение. Новые случаи заболевания COVID-19 учащаются с каждой минутой, и эксперты не знают, сколько времени пройдет, прежде чем эта пандемия будет взята под контроль. Между тем, потеря коммерции, торговли, туризма и глобальных цепочек поставок заставляет экономических экспертов бороться с пагубными последствиями, которые этот вирус будет иметь для мировой экономики в ближайшие годы. Мировая экономика предсказывала убыток в размере 280 миллиардов долларов в первом квартале года без срочных глобальных действий (47 ). Конференция Организации Объединенных Наций по торговле и развитию (ЮНКТАД) прогнозирует предварительный дефицит в 2 триллиона долларов в мировой экономике ( 48 ).
В ответ на пандемию COVID-19 FDA США продолжает свою работу по обеспечению безопасного и эффективного лечения. Потенциальные методы лечения, которые исследуются и разрабатываются для лечения и контроля COVID-19, в настоящее время включают многочисленные противовирусные препараты, иммунотерапию и вакцины ( 49 ). Противовирусный аналог нуклеотидов ремдесивир может ингибировать репликацию SARS-CoV и MERS-CoV во многих системах in vitro , таких как первичные культуры эпителиальных клеток дыхательных путей человека ( 50 , 51 ). Ремдесивир показал многообещающие результаты у макак-резусов, инфицированных SARS-CoV-2, и завершено испытание адаптивного лечения COVID-19 для ремдесивира, спонсируемое Национальным институтом аллергии и инфекционных заболеваний (ClinicalTrials.gov , NCT 04280705) ( 52 ). На основании этого исследования и исследования, спонсируемого Gilead ( ClinicalTrials.gov , NCT 04292899), FDA США разрешило экстренное применение ремдесивира для лечения COVID-19 ( 53 ). Было обнаружено, что лопинавир / ритонавир, ингибитор протеазы ВИЧ, ингибирует репликацию SARS-CoV-2 в клетках Vero E6 ( 54 ). Госпитализированные пациенты с COVID-19 в Ухане, Китай, получали комбинированную терапию лопинавиром / ритонавиром. Однако эффект был умеренным, и 13% пациентов пришлось удалить на ранних этапах лечения из-за неблагоприятных побочных эффектов ( 55). Новая комбинация тройной противовирусной терапии интерферона бета-1b, лопинавира-ритонавира и рибавирина при лечении пациентов с COVID-19 легкой и средней степени тяжести была безопасной и превосходила лечение только лопинавиром-ритонавиром в облегчении симптомов, сокращении продолжительности выделения вируса и пребывание в больнице. Однако отсутствие группы плацебо было одним из нескольких ограничений этого исследования ( 56 ).
CQ и его структурный аналог гидроксихлорохин (HCQ), одобренные FDA препараты, используемые в качестве противомалярийных средств с противовоспалительным и иммуномодулирующим действием, являются еще одним исследуемым препаратом противовирусной терапии, который перенаправляется и оценивается для лечения COVID-19. Исследования in vitro показали значительную активность CQ против SARS-CoV-2, SARS-CoV-1 и MERS-CoV ( 49 , 57 ). CQ является лизосомотропным агентом и ингибирует как эндосом и autophagosomal закисления, тем самым, ухудшая функциональность слитых эндосом-лизосомы, а также конденсированный аутофагос-лизосому (autolysosome) ( 58 — 60). CQ подавляет проникновение коронавирусной РНК в цитозоль, что необходимо для репликации вируса после эндоцитоза, опосредованного ACE2 ( рис. 1 ) ( 61 ). Доклиническое обоснование и доказательства перевели CQ в фазу клинических испытаний для лечения COVID-19. FDA одобрило экстренное использование CQ и HCQ для пациентов с COVID-19 ( 62 ). К сожалению, до сих пор не проведено крупное рандомизированное исследование, доказывающее, что эти препараты эффективны против этого заболевания. Интересно, что азитромицин и эритромицин, макролидные антибиотики, обладают специфическим противовирусным действием, которое может подавлять интернализацию вируса. Комбинированная терапия осельтамивиром и азитромицином использовалась в рандомизированных клинических испытаниях для лечения гриппа ( 63). Министерство здравоохранения Франции одобрило открытое нерандомизированное клиническое исследование HCQ-азитромицина на пациентах, инфицированных SARS-CoV-2, и показало многообещающие результаты в исследовании небольшого размера выборки ( 64 ). К сожалению, хорошо задокументировано, что аритмии представляют собой потенциальный риск у пациентов с COVID-19, получавших CQ-азитромицин ( 65 , 66 ).
Ремдесивир, лопинавир / ритонавир, CQ и азитромицин показали свою эффективность в подавлении репликации SARS-CoV-2 in vitro . Однако эффективность снижается, когда пациенты с симптомами проходят лечение через 1 неделю после начала заболевания. В этот момент пациент, возможно, уже перешел от вирусной экспансии к воспалительной фазе, ведущей к цитокиновому шторму ( 67 ). Например, во время заражения гриппом фаза выделения вируса достигает пика через 2–3 дня после заражения ( 68). Метаанализ рандомизированных контролируемых исследований осельтамивира (Тамифлю) показывает, что раннее лечение инфекции ускоряет облегчение клинических симптомов и снижает риски осложнений со стороны нижних дыхательных путей, что позволяет предположить, что лечение противовирусными препаратами должно быть правильно спланировано ( 69 , 70 ). Монотерапии противовирусными препаратами может быть недостаточно для тяжелых пациентов с COVID-19, и в качестве комбинированной терапии может потребоваться добавление противовоспалительных препаратов ( 71 ). Санофи и Регенерон объявили о фазе 2/3 испытания ингибитора интерлейкина-6 (ИЛ-6) сарилумаба (Кевзара) для уменьшения повреждения тканей легких, вызванного «цитокиновым штормом» у пациентов с инфекцией COVID-19 ( ClinicalTrials.gov, NCT 04315298) и Swedish Orphan Biovitrum (SOBI) также начали испытания фазы 2/3 Anakinra (антагонист рецептора IL-1) и Emapalumab (моноклональное антитело против IFN-γ), чтобы проверить их эффективность для уменьшения гипервоспалительного и респираторного дистресса у пациентов. пациенты с инфекцией COVID-19 ( ClinicalTrials.gov , NCT 04324021). В целом, предстоит провести больше клинических исследований, прежде чем какой-либо из этих препаратов станет общедоступным.
Также предпринимаются усилия по разработке вакцин против SARS-CoV-2. Основными вакцинами против COVID-19, которые подвергаются оценке, являются цельновирусные вакцины (вакцина с вектором аденовируса с использованием технологии AdVac и PER.C6 от Janssen), вакцины на основе рекомбинантных белковых субъединиц (технология рекомбинантных наночастиц от Novavax) и вакцины на основе нуклеиновых кислот (вакцина мРНК от Moderna / NIH. / CEPI) ( 72 ). Вакцина разработана в пандемической парадигме займет месяцы до нескольких лет , чтобы нести от стадии развития коммерциализации ( 72 — 74 ). Следовательно, необходим более быстрый и доступный подход к сдерживанию COVID-19. Из-за своих противовирусных свойств, доступности и одобрения FDA трегалоза заслуживает немедленной оценки как многообещающее профилактическое средство от COVID-19.
• Некоторые неспецифические противовирусные препараты проходят клинические испытания только в нескольких назначенных больницах. Хотя сроки выделения вируса SARS-CoV-2 хорошо известны, противовирусные препараты были бы более эффективными, если бы их вводили в начале заболевания. Более точные и быстрые диагностические тесты все еще находятся в стадии разработки, поскольку своевременная диагностика является ключом к лечению COVID-19 ( 75 ).
• Нет никаких лекарств или четких рекомендаций для бессимптомных или умеренно симптоматических пациентов с положительным результатом теста ( 76 , 77 ). Эти пациенты должны оставаться изолированными дома, что увеличивает шансы заразить других членов семьи.
• Страны, находящиеся в неблагоприятном социально-экономическом положении с некачественной системой медицинского обслуживания, окажутся в невыгодном положении по сравнению с США и некоторыми европейскими странами, которые проводят новейшие стратегии борьбы с COVID-19 ( 78 , 79 ). Крайне необходимы новые недорогие стратегии.
• Разработка вакцины началась в нескольких странах, но на это потребуется не менее 1 года.
• Бессимптомные пациенты могут получать ложноотрицательные результаты ПЦР, что приводит к недооценке положительных случаев COVID-19. Таким образом, это затрудняет попытки предотвратить распространение вируса внутри сообщества ( 80 ).
• Текущие меры блокировки могут ограничить распространение, но могут быть недостаточными для его полного прекращения.
Перспективы лечения трегалозой для немедленного сдерживания SARS-CoV-2
На сегодняшний день немедленные меры по предотвращению передачи SARS-CoV-2 сосредоточены на отслеживании контактов, карантине и социальном дистанцировании. Адаптация этих мер физического дистанцирования для смягчения последствий пандемии позволила сгладить кривую в некоторых странах ( 81 ). Города по всему миру начали заново открывать свою экономику; однако ожидается, что вторая волна случаев COVID-19 и летальных исходов начнется через 2–4 недели после повторного открытия ( 82 ). Постпандемическая динамика передачи повторных вспышек по проекту SARS-CoV-2 в зимний период и возобновление этой болезни могут сохраняться еще 3 года ( 83 ). Математическое моделирование различных сценариев с одноразовыми мерами социального дистанцирования смоделировало возобновление инфекции, когда меры социального дистанцирования были отменены (83 ). Таким образом, необходимы дополнительные методы, позволяющие избежать принудительного социального дистанцирования и остановки экономики. В качестве альтернативы пути к коллективному иммунитету потребуют либо массовой вакцинации, либо естественной иммунизации с течением времени. Однако последний подход предполагает, что большая часть населения умрет от болезни ( 84 ). R 0 , базовое репродуктивное число, представляет собой передаваемость инфекционных агентов в наивной популяции и может варьироваться в зависимости от динамики передачи ( 85 ). Таким образом, R 0 различается в разных популяциях. R 0 SARS-CoV-2, как сообщалось, находится в диапазоне от 1,4 до 6,49 в недавних исследованиях с января 2020 года по февраль 2020 года ( 86). При R 0, равном 6,49, населению потребуется, чтобы у 85% людей был иммунитет, чтобы сдерживать распространение болезни, 1 — 1 / R 0 . Неизвестно, сколько времени потребуется различным популяциям для приобретения коллективного иммунитета из-за факторов динамики передачи, таких как демография, культурные влияния, частота контактов и плотность населения ( 87 ). Таким образом, нацеливание на лиц, которые считаются малорисковыми, может создать защиту сообщества для защиты тех, кто уязвим, но не имеет иммунитета.
Мы предлагаем трегалозу как практичное и доступное безопасное средство для профилактики и сдерживания COVID-19. Трегалоза потенциально может повлиять на клеточные органеллы, необходимые для репликации вируса. Мы бы порекомендовали крупное общественное исследование, включающее здоровых взрослых, медицинских работников, бессимптомных пациентов и пациентов с легкими симптомами COVID-19 ( рисунок 2 ). Центры по контролю за заболеваниями (CDC) недавно сообщили о передаче SARS-CoV-2 на пресимптомной стадии инфекции; поэтому лечение трегалозой в качестве профилактического подхода было бы целесообразно ( 88 , 89). Членам семей пациентов с положительным результатом на COVID-19 будет рекомендовано пройти курс лечения трегалозой и оставаться дома в условиях карантина, поскольку частота вторичных атак при передаче SARS-CoV-2 в семье составляет 16,3% ( Рисунок 2 ) ( 90 ). В отличие от взрослых, у детей низкая заболеваемость COVID-19. У детей в большинстве случаев бессимптомное течение или симптомы легкие, требующие медицинской помощи, если не существует основного состояния, наносящего ущерб здоровью ( 91 , 92 ). Совсем недавно детские больницы подтверждают случаи детей, страдающих тяжелой болезнью Кавасаки, связанной с COVID-19 ( 93). Это вызывает серьезную озабоченность, когда страны пытаются вновь открыть свою систему образования, а долгосрочные последствия инфекции SARS-CoV-2 у детей до сих пор неизвестны. Клинические исследования перорального приема трегалозы (100 г / день) для улучшения функции сосудов проводились у здоровых взрослых людей в возрасте 50–77 лет ( 94). Несмотря на то, что трегалоза оказалась безопасной, она была бы неуместной или подходить с осторожностью при оценке эффективности трегалозы у пожилых людей и пожилых людей, поскольку большая часть этой группы населения страдает хроническими заболеваниями. Если лечить здоровых взрослых трегалозой, резистентность к инфекции на популяционном уровне блокирует цепь передачи. В результате этого лечения риск передачи инфекции пожилым людям и лицам с ограниченными возможностями здоровья будет резко снижен, поскольку они косвенно защищены от инфекции ( рис. 2 ) ( 95 ). Кроме того, трегалоза может активировать TFEB и впоследствии способствовать перекрестной презентации ( 18 , 19). Следовательно, трегалоза может иметь еще одно преимущество для повышения коллективного иммунитета против SARS-CoV-2, особенно на этапе столкновения со второй волной случаев COVID-19. Мы считаем, что эта стратегия лечения может быть более выгодной для стран, у которых нет ресурсов для проведения клинических испытаний противовирусных препаратов.ФИГУРА 2
Рисунок 2 . Лечение трегалозой для быстрого сдерживания SARS-CoV-2. Лечение трегалозой здоровых взрослых и бессимптомных пациентов ускорит локализацию вирусов в сообществе.
Возможные меры предосторожности и текущие ограничения для разработки лечения трегалозой
Важно понимать, что, несмотря на обширные исследования применения трегалозы у взрослых, все еще недостаточно данных о ее безопасности для детей, взрослых с проблемами, связанными со здоровьем, и пожилых людей. Ранее мы сообщали, что трегалоза обостряла острый респираторный дистресс-синдром (ARDS) на мышиной модели «двух ударов» (индуцированный LPS и механической вентиляцией легких), в то время как другие активации аутофагии подавляли ARDS ( 96 ). Таким образом, лечение трегалозой было бы неприемлемым для лечения пациентов интенсивной терапии с тяжелой формой COVID-19, особенно тех, у кого наблюдается синдром цитокинового шторма или ОРДС. Для воспалительных цитокинов было показано, что трегалоза подавляет LPS-индуцированную секрецию IL-1β и TNF-α в перитонеальных макрофагах мыши ( 97 ). Наш экспериментальный in vitroданные показывают, что предварительная обработка трегалозой ингибировала индуцированную LPS продукцию IL-6 в макрофагах (неопубликовано). Как и в клинических рекомендациях общества инфекционистов Америки по ведению гриппа, раннее лечение противовирусными препаратами ослабляет симптомы и снижает риск возникновения осложнений. Таким же образом трегалоза может иметь более значительное противовоспалительное действие на начальной стадии инфекции SARS-CoV-2. Лечения тяжелых пациентов с COVID-19 на поздней стадии заболевания будет недостаточно. Вместо этого другие экстренные фармацевтические вмешательства, одобренные FDA, будут более эффективными. Хотя трегалоза может обеспечить значительные преимущества в качестве противовирусного лечения, исследования показали, что диетическая трегалоза может повышать вирулентность Clostridium difficile (98 ). Исследования in vitro воздействия трегалозы на инфекцию SARS-CoV-2 все еще нуждаются в изучении, поскольку некоторые типы вирусов могут нарушать работу системы аутофагии и усиливать свою репликацию при лечении трегалозой (например, ВСР) ( 36 ). После подтверждения эффективности трегалозы тесты на модели макаки-резус будут идеальными для определения подходящей начальной дозы для клинических испытаний на людях. В большинстве случаев введение трегалозы взрослым составляет от 4,8 до 10 г / день. Изменение аутофагии в легких было подтверждено при использовании 1 г / кг трегалозы для мышей, что эквивалентно 4,8 г / день на каждые 60 кг у человека ( 96 ). В исследовании диабета использовалось 10 г / день ( 8), в то время как в клиническом исследовании острой коронарной артерии использовалось 2,1 г / день ( ClinicalTrials.gov , NCT 03700424). Доза 30 г использовалась для слабительных целей у здоровых женщин ( 3 ). Эффективная доза трегалозы на массу тела для нацеливания на SARS-CoV-2 и фармакокинетику трегалозы в крови человека еще предстоит определить. Следует отметить, что голодание между 16 и 18 часами также активирует аутофагию; однако, как сообщалось ранее, это не лучшая стратегия лечения вирусной инфекции ( 99 ). Таким образом, мы не рекомендуем голодание как профилактическое средство от COVID-19. Рапамицин, типичный mTOR-зависимый активатор аутофагии, оказывает иммуносупрессивное побочное действие, что может сделать его неадекватным для профилактического лечения SARS-CoV-2 ( 15 ).
Поскольку SARS-CoV-2 продолжает расширяться во всем мире, крайне важно получить знания и понимание его воздействия на разрозненные сообщества. Предлагаемое лечение трегалозой потенциально может защитить тех, кто не может искать более дорогостоящие лекарства. Поскольку исследования и испытания COVID-19 продолжаются бесконечно, а экономика страдает, следует рассмотреть более экономичные варианты для быстрого сдерживания. Исследование более безопасных методов лечения вирусных инфекций должно быть постоянным приоритетом, поскольку пандемия COVID-19 не будет последней в своем роде. Мы предлагаем трегалозу для рассмотрения в агентствах общественного здравоохранения во всем мире.