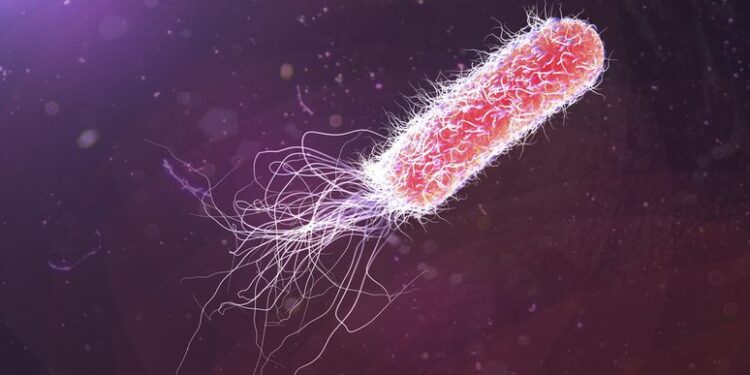
Штамм бактерий, распространенный у пациентов с SPMS, также поддерживает связь с прогрессированием.
Исследование показало, что определенные виды бактерий обогащаются в кишечнике людей со вторичным прогрессирующим рассеянным склерозом (SPMS) и могут способствовать развитию нейровоспаления и прогрессированию инвалидности у этих пациентов.
При выделении у пациентов с SPMS и введении мышиной модели этот штамм приводил к более выраженной неврологической инвалидности и увеличению количества иммунных клеток, непосредственно участвующих в воспалении, которое вызывает рассеянный склероз (MS).
Исследователи предполагают, что этот вид бактерий способствует воспалению благодаря активности своих жгутиков, волоскообразных выступов, которые помогают бактериям перемещаться, прилипать и проникать в клетки-мишени.
Из-за продолжающейся патентной защиты исследователи не смогли раскрыть название бактерий, назвав его “бактерии X”.
Исследование различий в микробиоме кишечника между типами РС, переход болезни
“Избирательное устранение патогенных бактерий, включая эту бактерию X, может привести к инновационным методам лечения пациентов с SPMS”, — сказал Дайки Такеваки, доктор медицинских наук, в презентации “Идентификация патогенных кишечных бактерий, лежащих в основе прогрессирования рассеянного склероза”.
Такеваки из Национального центра неврологии и психиатрии в Японии представил результаты на Форуме Американского комитета по лечению и исследованиям рассеянного склероза (ACTRIMS) 2023, который состоялся 23-25 февраля в Сан-Диего.
Растущее количество доказательств связывает микробиом кишечника — миллиарды бактерий, грибков и вирусов, живущих в кишечном тракте, — с нарушением иммунной регуляции при рассеянном склерозе. Нарушения в балансе этих микробов обычно наблюдаются у пациентов с РС, а изменения в кишечных бактериях связаны с более ранним и более тяжелым заболеванием на животных моделях РС.
Однако, как микробиом кишечника различается между типами рассеянного склероза и могут ли определенные бактерии быть ответственны за переход от рецидивирующего к прогрессирующему течению заболевания, до сих пор неясно.
Существует ли «причинно-следственная связь между дисбактериозом кишечника и прогрессированием РС … [также] остается неуловимым ”, — написали исследователи, добавив, что, если такая взаимосвязь будет подтверждена, конкретные “бактерии, вызывающие заболевание”, еще предстоит идентифицировать.
Такеваки и его команда ранее проанализировали образцы кала у пациентов с рецидивирующим ремиттирующим РС (RRMS) и SPMS, обнаружив особый профиль микробиома, связанный с каждым типом РС.
Теперь они стремились идентифицировать конкретные кишечные бактерии, связанные с прогрессированием РС, и вероятные механизмы, которые вызывают нейровоспаление.
Используя бактериальную ДНК, полученную в образцах кала от 62 RRMS и 15 пациентов с SPMS, исследователи обнаружили 12 видов бактерий, которые были особенно обогащены в образцах SPMS. Из них уровни бактерий X показали самую сильную корреляцию с уровнями инвалидности пациентов, оцененными с использованием расширенной шкалы статуса инвалидности (EDSS).
Геномные данные из общедоступных баз данных Международного консорциума генетиков рассеянного склероза (IMSGC) подтвердили относительное увеличение бактерий X среди людей с прогрессирующим рассеянным склерозом, особенно у пациентов с оценкой EDSS от 3 до 5, что указывает на инвалидность от средней до тяжелой степени.
Это наблюдение «подтверждает, что бактерии X сильно обогащены на прогрессирующей стадии РС», — сказал Такеваки.
При дальнейшем исследовании были идентифицированы два разных штамма или подтипа бактерий X. В то время как уровни штамма A1 были одинаковыми среди здоровых людей и пациентов с RRMS и SPMS, штамм B1 был значительно более распространен в образцах SPMS по сравнению с двумя другими группами.
Затем исследователи работали с мышами, у которых отсутствовали все микроорганизмы, называемые мышами без микробов. Эти животные обычно устойчивы к неврологическим нарушениям, которые характеризуют экспериментальный аутоиммунный энцефаломиелит (EAE), распространенную мышиную модель рассеянного склероза.
Значительное увеличение инвалидности наблюдается у мышей, получавших штамм B1 от пациентов с SPMS
Когда штамм B1 бактерий X, выделенный от пациентов с SPMS, был доставлен мышам без микробов, их инвалидность значительно увеличилась. Аналогичная степень инвалидности не наблюдалась, когда штамм бактерий A, выделенный у пациентов с RRMS, давали этим мышам.
Бактерии, полученные из SPMS, также привели к относительному увеличению клеток Th17, типа провоспалительных иммунных клеток, которые считаются основной причиной воспаления при РС, в толстом кишечнике и головном мозге. Штамм A также приводил к значительному увеличению этих клеток, хотя и в меньшей степени.
Изучая различия между штаммами A1 и B1, которые могут объяснить более тяжелые механизмы заболевания бактериями, полученными из SPMS, команда обнаружила, что штамм B1 экспрессировал больше генов, связанных со жгутиками. Под микроскопом было обнаружено, что у этих бактерий есть жгутикоподобные структуры, и они прикрепляются к клеткам толстой кишки.
“После переноса бактерий мышам без микробов мы подтвердили, что бактерии X штамма B1 могут колонизировать толстую кишку пересаженных мышей”, — сказал Такеваки.
Примечательно, что считается, что определенные типы жгутиков у бактерий активируют рецепторы, называемые toll-подобными рецепторами 5 (TLR5). Это вызывает высвобождение провоспалительной молекулы интерлейкина-6 (IL-6) из определенных иммунных клеток, которые, в свою очередь, активируют клетки Th17.
Исследователи отметили, что это может быть одним из способов, которым бактерии X способствуют воспалению в SPMS, и поддержали в экспериментах. В частности, бактерии, полученные из SPMS, значительно стимулировали активность TLR5 в клеточных культурах и способствовали секреции IL-6 из иммунных клеток.
Это повышение уровня IL-6 было подавлено в присутствии молекулы, которая блокирует toll-подобный рецептор 5.
“Мы подтвердили, что бактерии X способны индуцировать клетки Th17 в кишечнике и впоследствии усугублять воспаление нейронов”, — сказал Такеваки, добавив, что это “возможно, связано с прогрессированием заболевания от RRMS до SPMS”.