Моя цель лечения NEIDA (Нет свидетельств активности тлеющего воспаления болезни) для моих пациентов с MS. Новый акцент делается на предотвращении повреждения конечных органов. Для достижения этой цели мы должны признать, что Фарм. промышленность ослепила (одурачила) нас. Наша цель лечения должна быть тлеющей MS,т.е. остановка прогрессирования инвалидности, нормализация потери объема мозга, уплощение уровня нейрофиламента, остановить медленно расширяющиеся поражения, очистка ЦСЖ от олигоклональных полос и, если возможно содействия восстановлению нервной системы.
Что хорошего в том, чтобы быть просто свободным от рецидивов и новых очагов на МРТ, если вам все равно медленно становится хуже? Вот почему концепция использования низкой дозы анти-CD20 терапии так недостаточна. Ясно, что испытуемые подвергались более низким дозам окрелизумаб в фазе 3 испытаний, а также тех, кто подвергается более высоким дозам в связи с рецидивами и МРТ активности, но не в связи с ухудшением инвалидности (см. слайд-шоу ниже).
Из этого пост-специального анализа, ясно, что вам нужно высокие, а не низкие, дозы анти-CD20 терапии по крайней мере первоначально в качестве индукционной стратегии для очистки различных В-клеточных отсеков. Мы предполагаем, что в этих отсеках B-клеток находится клетки памяти, которые могут быть средой обитания для скрытого EBV и/или высоко аутореактивной популяции B-клеток, которые управляют и поддерживают MS-заболевание. Эта популяция клеток может находиться в глубоких тканях и/или центральной нервной системе. Вот почему мы и другие тестируем КНС пенетант анти-B-клеток стратегии (ixazomib, кладрибин, ингибиторы BTK и т.д.), т.е. нацеленную на максимальное проникновение в ЦНС.
Тем не менее, я предположил, что как только вы очистили эти отсеки В-клеток, скажем, после двух лет лечения вам больше не придется поддерживать такие высокие дозы анти-CD20 терапии, которая подавляет нормальные B-клетки и их роль в биологии и иммунных реакций, которые приводят к долгосрочным осложнениям. Вот почему я предложил использовать окрелизумаб в качестве иммунной терапии восстановления, т.е. сперва получить высокие дозы затем перерыв в лечении и ждать, чтобы увидеть, если MS остается в ремиссии или болезнь возвращается и требует дополнительных курсов. Последнее мы предлагаем сделать в исследовании ADIOS.
Еще лучше было бы два года индукционной терапии с высокодозным окрелизумаб далее следует поддерживающая терапия, такая как териономид, лефтономид, ИДУ-838 (vidofludimus) или ASLAN003 (селективные ингибиторы DHODH второго поколения), HAART (высоко активные антиретровирусные препараты), фамцикловир или другой анти-EBV вирусный агент.
Гипотеза заключается в том, чтобы позволить B-клеткам восстановится после анти-CD20 терапии в присутствии противовирусного агента для предотвращения Реактивации EBV и повторной инфекции новых В-клеток памяти. Делая это вы также будете снижать риски долгосрочной иммуносупрессии, связанные с анти-CD20 терапии и предотвратить развитие гипогамаглобулиномии. Эта стратегия также позволит пациентам реагировать на вакцины.
Однако, если вы хотите более низкую дозу анти-CD20 терапии вы сможете начать очень скоро Ofatumumab. Пожалуйста, помните о Ofatumumab он значительно превосходит терифлюномид в подавлении рецидивов, но хуже терифлюномида при замедлении потери объема мозга в год два ASCLEPIOS I и II клинических испытаний (NCT0279218 и NCT02792231). почему?
Ниже приводится фундаментальный вопрос, который вы должны задать себе.
Так что бы вы выбрали для лечения MS
с; (1) низкие дозы анти-CD20, (2) высокие дозы анти-CD20, (3) высокие дозы анти-CD20 терапии с последующим обслуживанием или (4) иммунно-реконституционной терапии (кладрибин, алемтузумаб или AHSCT)?
Уныно мы не можем предложить все из этих выборов к всем из наших пациентов с MS в настоящее время
NHS.
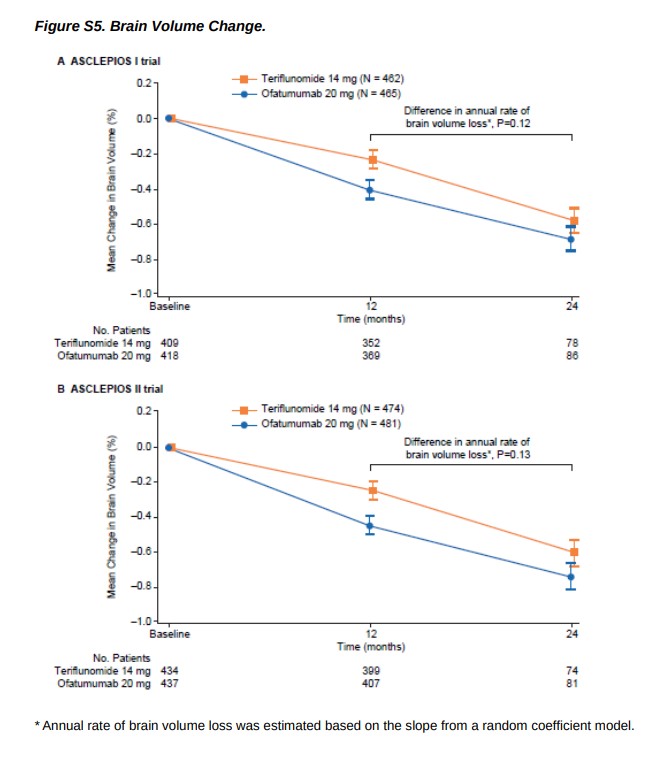
Хаузер и др. Ofatumumab против терифлюномида при рассеянном склерозе. N Engl J Med. 2020 Авг 6;383(6):546-557. Справочная информация : Ofatumumab, подкожное анти-CD20 моноклональных антител, избирательно истощает В-клеток.
Терифлюномид, пероральный ингибитор синтеза пиримидина, уменьшает активацию Т-клеток и В-клеток. Относительные последствия этих двух препаратов у пациентов с рассеянным склерозом не известны. Методы : В двух двойных слепых, двойной манекен, фаза 3 испытаний, мы случайно назначенных пациентов с рецидивирующий рассеянный склероз, чтобы получить подкожный ofatumumab (20 мг каждые 4 недели после 20-мг получения дозы в дни 1, 7 и 14) или перорально терифлуномида (14 мг в день) на срок до 30 месяцев.
Основной точкой является годовой уровень рецидивов. Вторичные конечные точки включали ухудшение инвалидности подтверждено на 3 месяца или 6 месяцев, улучшение инвалидности подтверждено в 6 месяцев, количество гадолиния повышения поражений на T1 взвешенных магнитно-резонансной томографии (МРТ) сканирование, годовой уровень новых или увеличения поражений на T2 взвешенных МРТ, сыворотки нейрофиламента цепи уровнях в 3 месяца, и изменение объема мозга. Результаты : В целом, 946 пациентов были назначены для получения ofatumumab и 936 для получения терифлюномида;
средний срок последующей деятельности составил 1,6 года. Годовые показатели рецидивов в группах ofatumumab и teriflunomide составили 0,11 и 0,22, соответственно, в пробной версии 1 (разница, -0,11; 95% интервал доверия ,CI), -0,16 до -0,06; P<0.001) и 0.10 и 0.25 в пробе 2 (разница, -0.15; 95% CI, -0.20 до -0.09; P<0.001). В объединениях испытаний, процент пациентов с инвалидностью ухудшение подтверждено в 3 месяца было 10,9% с ofatumumab и 15,0% с терифлюномид (коэффициент опасности, 0,66; Р 0,002 евро); процент ухудшения состояния инвалидности, подтвержденный в 6 месяцев, составил 8,1% и 12,0%, соответственно (коэффициент опасности, 0,68; Р 0,01); и процент с улучшением инвалидности подтвердил в 6 месяцев составил 11,0% и 8,1% (коэффициент опасности, 1,35; No 0,09). Количество гадолиний повышения поражений на T1 взвешенных МРТ, годовой уровень поражений на T2 взвешенных МРТ, и сыворотки нейрофиламента световой цепи уровнях, но не изменение объема мозга, были в том же направлении, как основная точка конца. Реакции, связанные с инъекциями, происходили в 20,2% в группе ofatumumab и в 15,0% в группе терифлюномида (инъекции плацебо). Серьезные инфекции произошли у 2,5% и 1,8% пациентов в соответствующих группах. Выводы : Среди пациентов с рассеянным склерозом, ofatumumab был связан с более низкими годовыми показателями рецидивов, чем терифлуномид.
(Финансируется Novartis; ASCLEPIOS I и II ClinicalTrials.gov номера, NCT02792218 и NCT02792231.).