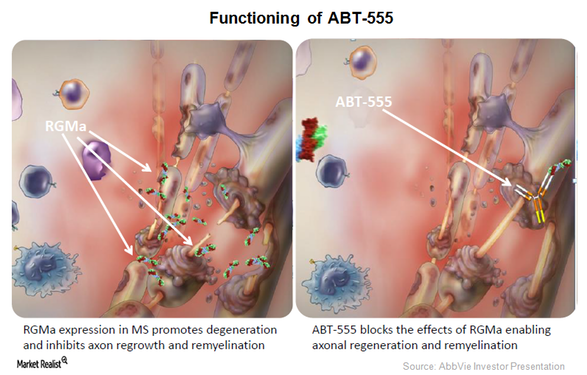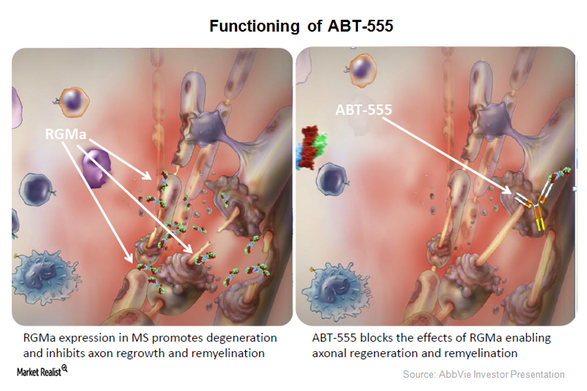
Элезанумаб — полностью гуманизированное моноклональное антитело, направленное против отталкивающей направляющей молекулы А (RGMa). Исследования на пациентах с рассеянным склерозом (РС) демонстрируют повышенную регуляцию RGMa, которая ингибирует рост аксонов и миелинизацию, олигодендроглиальную регенерацию и функциональное восстановление после травмы или воспаления. Лечение Элезанумабом способствовало регенерации аксонов, нейропротекции, ремиелинизации и иммунной модуляции в нескольких предклинических состояниях, связанных с МС Модели.1. Элезанумаб ранее назначался в виде однократной дозы здоровым добровольцам и хорошо переносился. В этом исследовании оценивались множественные дозы элезанумаба для определения его безопасности и переносимости у пациентов с рецидивирующими формами РС.
Методы: в этой фазе 1, двойное слепое, плацебо-контролируемое, рандомизированное, возрастающее многодозовое 29-недельное исследование, пациенты были рандомизированы на 3 группы лечения и 1 группу плацебо. Из 20 пациентов (12 женщин, 8 мужчин) 18 имели ремиттирующий РС и 2 имели вторичный прогрессирующий РС. Дозы элезанумаба вводились внутривенно каждые 4 недели в общей сложности для 4 доз, причем нагрузочная доза в два раза превышала поддерживающую дозу, полученную в день 1. Поддерживающие дозы составляли 150 мг, 600 мг и 1800 мг элезанумаба для групп 1, 2 и 3. соответственно. Оценки включали нежелательные явления, возникающие при лечении (TEAE), анализ спинномозговой жидкости (ЦСЖ) и плазмы, а также анализ биомаркеров плазмы и расширенный показатель инвалидности (EDSS). Впоследствии будут представлены данные магнитно-резонансной томографии и фармакокинетики сыворотки.
Результаты. Наиболее частым случаем TEAE была головная боль (25% всех пациентов). Свободнорастворимый RGMA снижался с увеличением уровней элезанумаба в CSF, в то время как общий RGMA (как свободный, так и связанный с антителами) линейно увеличивался при воздействии элезанумаба в CSF. Интерлейкин-10 также увеличился в CSF после введения элезанумаба по сравнению с плацебо. С начала и до конца периода наблюдения большинство пациентов, получавших элезанумаб, не испытывали клинически значимого ухудшения или улучшения показателей EDSS.
Выводы: Elezanumab хорошо переносился и не приводил к ухудшению симптомов у пациентов, которые получали многократные дозы до 1800 мг. Дополнительные долгосрочные исследования необходимы для выяснения эффективности элезанумаба в более здоровой популяции пациентов.
Рекомендации:
- Мюллер Б.К. и соавт. Mult Scler J. 2015; 21 (S11): 76-653. Плакат № 582.
- Cree BAC, et al. Mult Scler J. 2016; 22 (S3): 400-705. Плакат № 1209.
Раскрытие информации: BACC получил гонорары за консультационные услуги от AbbVie, Inc., Akili, Biogen, EMD Serono, GeNeuro, Novartis и Sanofi Genzyme. MR, BB и AZ являются штатными сотрудниками AbbVie и могут владеть акциями и / или опционами на акции. AbbVie, Inc. финансировала это исследование и участвовала в разработке исследования, исследовании, сборе данных, анализе и интерпретации данных, а также написании, рецензировании и утверждении данного реферата для презентации. Все авторы имели доступ к данным; участвовал в разработке, рецензировании и утверждении реферата; и согласился представить этот тезис в ECTRIMS для рассмотрения. Авторы хотели бы поблагодарить доктора философии Томаса П. Миско за его вклад в реферат. Редакционная помощь предоставлена Дженнифер Драйер, доктор философии, и Кристи А. Грабовски, доктор философии, Дж. Б. Аштин; финансируется AbbVie, Inc.