Вероятно, существует много других важных вопросов, связанных с этиологией «прогрессирующей нейродегенерации» при рассеянном склерозе. Заманчиво согласиться с тем, что РС представляет собой нейродегенеративное заболевание ЦНС с пост-активированными характеристиками иммунной системы, а не предустановленный аутоиммунитет, который вызывает воспалительный каскад заболевания (РС или Оптико неврита) с нейродегенеративными характеристиками. Хотя воспаление может быть частично вовлечено, разумно предположить, что это может быть компенсаторная иммунная реакция, в первую очередь направленная на очищение от остатков миелина, а не на поврежденные нейроны, изначально присущие, как возможный механизм восстановления после начала триггерной точки демиелинизации. Напротив, ингибирование этого механизма восстановления может ускорить атрофию головного мозга и частые рецидивы.
Патогенные механизмы рассеянного склероза включают биохимические модификации различных белков, встроенных в аксональные слои олигодендроцитов, такие как перекисное окисление липидов и липокисление белков [ 55 ]. Кроме того, патология РС поражает белое вещество и серое вещество, и изнурительные клинические результаты коррелируют с общим нейродегенеративным процессом [ 52 ]. Эти наблюдения требуют отправной точки для начала клинических исследований рассеянного склероза и ПО на основании научных обоснований и выводов из традиционных доклинических моделей на основе иммунитета.
Таблица 1. Влияние глюкокортикоидов на модели РС и Оптико неврита у животных и клеток.
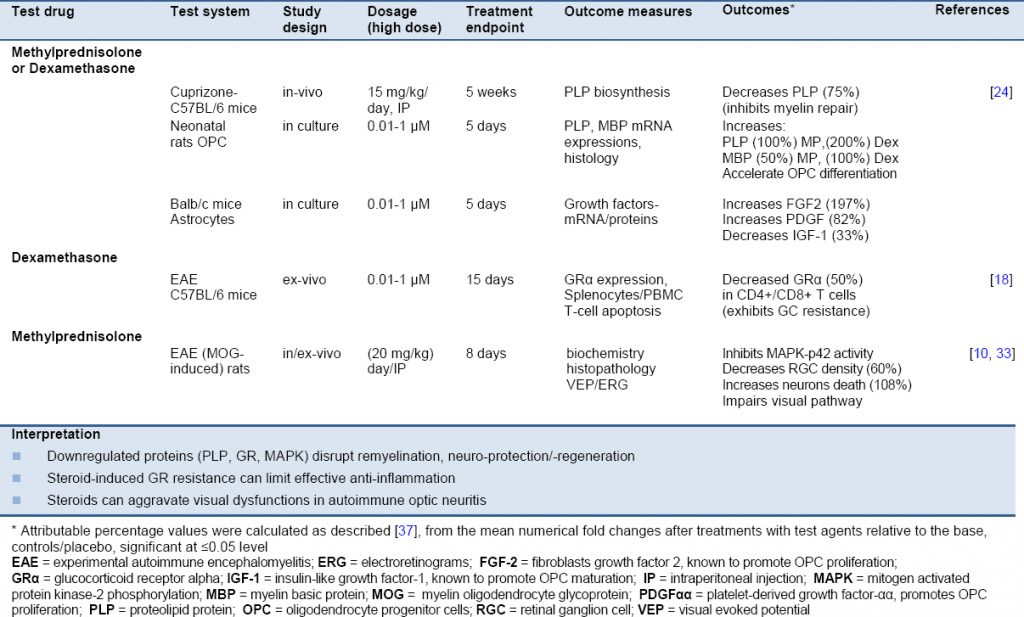
Может ли лечение стероидами помочь или препятствовать нейрогенезу, в частности восстановлению миелина? Противоречивые недавние наблюдения показывают, что Глюкокортикоиды препятствуют пролиферации и / или созреванию олигодендроцитов и биосинтезу факторов роста в астроцитах. Этот эффект может подавлять дифференцировку клеток-предшественников олигодендроцитов (OPC), ингибировать спонтанное восстановление миелина в модели неиммунного купризон-индуцированного повреждения у животных. Кроме того, в дополнение к иммуносупрессии, Глюкокортикоиды могут изменять биосинтез и высвобождение факторов роста / дифференцировки и препятствовать восстановлению миелина [ 24 ] ( Таблица 1).). Непротиворечивость ассоциации этих результатов также имеет отношение к правдоподобию связанных с лечением Глюкокортикоедов возмущения оси HPA, подавления экспрессии GR в астроцитах, ингибирования пролиферации и уменьшения числа астроцитов в коре — поддерживается на модели животных, как а также клетки в культуре [ 27]. Эти результаты могут также иметь отношение к поражениям серого вещества у пациентов с РС, получавших Глюкокортикоиды.
Уменьшение количества астроцитов кортикостероидами может быть в пользу реактивного глиоза или глиального рубца, хотя возможно также за счет сокращения полезной роли астроцитов в очистке миелиновых остатков [ 28 ]. У пациентов с РС с признаками продолжающегося воспаления, что неудивительно, хотя лимфоциты могут приобретать устойчивость к Глюкокортикоидам [ 18 ]. То, влияют ли фармакологические глюкокортикостероиды на пролиферацию / миграцию клеток-предшественников олигодендроцитов и влияют ли они на функциональное восстановление поврежденных нейронов в среде поражения, является экспериментально обоснованной проблемой безопасности — разумной гипотезой ( рис. 2 ).
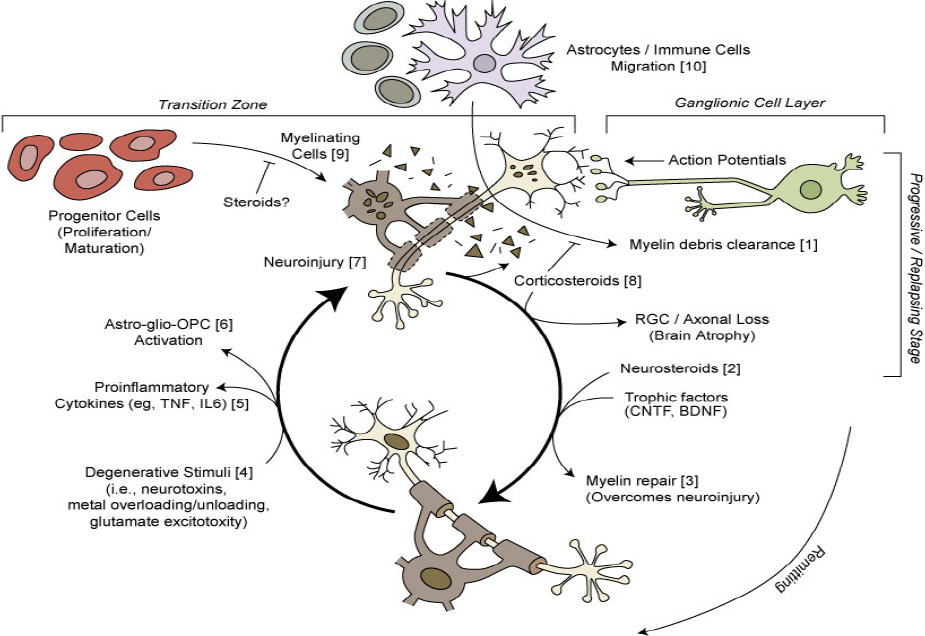
Рисунок 2. Влияние стероидов на цикл де/ремиелинизации проиллюстрировано в отношении механизмов заболевания при RRMS и MS-ON. Взаимосвязь между вредными нейронами и ганглиозными клетками и регенеративным ответом может включать в себя множественные типы клеток и эндогенные клеточные модуляторы в ЦНС; выделенные элементы, включая противоположные полезные (1,2,3,6,9,10) и опасные (4,5,7,8) ступени при травме нервной системы, а также эффекты эндогенных и экзогенных стероидов. В то время как фармакологические стероиды могут ослаблять инфильтрированные иммунные клетки и разрушать воспаление, они также могут вызывать ингибирующие / проапоптотические эффекты, приводящие к глубоким изменениям плотности невритов и дендритов, репаративной потере аксонов и атрофии головного мозга.
Заключение
Лечение, основанное на предположении, что деградация, вызванная воспалением, является единственным механизмом прогрессирования заболевания, неубедительно. Важно отметить, что выводы сделанные на основе модели аутоиммунного энцефаломиелита (ЭАЭ) у мышей в качестве научных обоснований для обоснования подходов к лечению у людей, могут быть ошибочными! Приписывание причин ухудшения поражения индуцированной стероидами прогрессирующей атрофии в отделах серого вещества и мозжечка трудно исключить, основываясь на имеющихся данных. Кроме того доказательства подтверждающие пользу стероидов для уменьшения воспаления для улучшения ганглиозных клеток сетчатки на животных моделях неврита зрительного нерва, также неубедительны. Модифицированные подходы, основанные на фактических данных, а не на экстраполяции за пределами диапазона данных, необходимы для:
i) предотвращения или уменьшения распространения атрофии в ЦНС.













Здравствуйте.
Простите, а эта информация факт или домысел? Если Факт, то можно ещё какую-нибудь ссылочу на этот материал. (можно и не на русском, если оригинал на другом языке).
Заранее спасибо.
http://www.jecns.com/JECNS/article/view/9/49