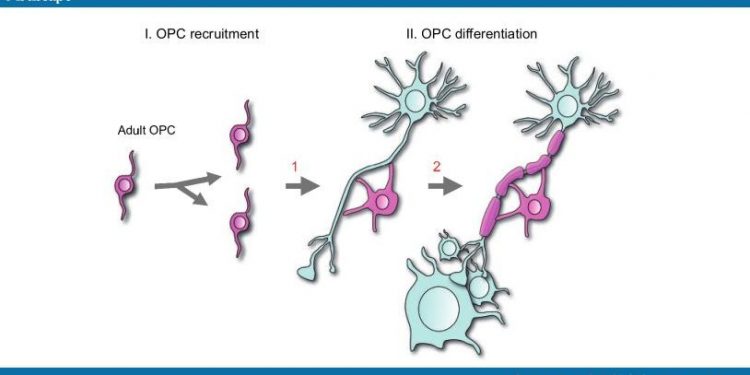
Современные методы лечения рассеянного склероза (МS) эффективны для снижения частоты рецидивов, краткосрочных показателей инвалидности и показателей воспаления с помощью магнитно-резонансной томографии (МРТ) при рецидивирующем ремиттирующем МS (RRMS), тогда как в фазе прогрессирующего / дегенеративного заболевания эти препараты имеют мало или нет выгоды. Поэтому разработка новых методов лечения направленных на реверсирование нейродегенерации, представляет большой интерес. Ремиелинизация которая обычно является спонтанным эндогенным процессом, достигается когда миелин-продуцирующие олигодендроциты генерируются из клеток-предшественников олигодендроцитов (OPCs). Хотя эти клетки-предшественники в изобилии присутствуют в мозге МS, их способность к регенерации ограничена. Поэтому усиление генерации миелин-продуцирующих клеток является основным направлением исследований РС.
Современные методы ремиелинизации
Современные методы лечения MS в первую очередь иммуномодулируют и эффективно снижают частоту рецидивов и показатели воспаления с помощью магнитно-резонансной томографии (МРТ). Помимо выявления потенциальных лекарств, вызывающих репарацию миелина, в базовых исследованиях и клинических испытаниях, исследующих регенеративные соединения, исследования также были направлены на выявление дополнительных регенеративных свойств существующих лекарств, используемых для других показаний.
Ремиелинационная терапия в клинических испытаниях
Клемастин
Клемастин, блокатор рецепторов гистамина H1 первого поколения, был идентифицирован как потенциально ремиелинизирующий препарат при высокопроизводительном скрининге in vitro. Его ремиелинизирующий эффект был подтвержден, в результате чего в клиническом исследовании в 50 больных (RRMS перестраивать, NCT02040298). Эффект перорально вводимого клемастина на хроническую демиелинизирующую оптическую невропатию был исследован с использованием сокращения задержки латентности P100 в визуально вызванных потенциалах (VEP). Было обнаружено что препарат снижает латентность P100 на 3,2 мс / глаз, если результаты исследования были проанализированы как «испытание с отсроченным лечением» или 1,7 мс / глаз, если рассматривать его как «перекрестное исследование».
GSK239512
Это перорально вводимое антигистаминное лекарственное средство, проникающее в ЦНС, которое нацелено на рецептор H 3 первоначально было разработано для лечения шизофрении и болезни Альцгеймера но было обнаружено что оно неэффективно для этих показаний. Эффективность GSK239512 для ремиелинизации была протестирована в рандомизированное рандомизированное исследование с малой фазой в параллельных группах, плацебо-контролируемое двойное слепое международное многоцентровое исследование взрослых с RRMS (NCT01772199). В то время как препарат хорошо переносился, к сожалению испытание не смогло достичь его первичных и вторичных конечных точек. Однако в последующем анализе с использованием коэффициента переноса намагниченности (MTR) для оценки содержания миелина in vivo обработка GSK239512 привела к небольшим средним улучшениям пораженного MTR по сравнению с плацебо.
Опицинумаб
Опицинумаб — это антитело, направленное против белка, богатого лейцином, и белка 1, взаимодействующего с рецептором Nogo (LINGO-1), содержащего иммуноглобулин-подобный домен, трансмембранного белка, экспрессирующегося исключительно в ненейрональных клетках ЦНС. Специфическая потеря LINGO-1 in vitro, а также in vivo усиливает образование миелиновой оболочки и миелинизацию и было обнаружено, что применение специфических антител против LINGO-1 снижает тяжесть EAE. В двух исследованиях была исследована эффективность опицинумаба при неврите зрительного нерва (ПО ) и RRMS (NCT01864148) соответственно. Исследование RENEW в ON показало улучшение в восстановлении латентности зрительной нервной проводимости, измеренной с помощью VEP, в то время как исследование SYNERGY не достигло своей основной конечной точки. Тем не менее, на основе анализа post hoc, выявляющего повышенный клинический эффект в подгруппе пациентов (РС не более 20 лет и базовая МРТ, свидетельствующая об относительной потере миелина и большей структурной целостности), было начато продолжающееся исследование AFFINITY, которое ориентировано больше к лучше отвечающей популяции (NCT03222973).
GNbAC1
GNbAC1, который является гуманизированным антителом, направленным против белка оболочки (ENV) ретровируса, связанного с рассеянным склерозом (MSRV), является еще одним кандидатом, вероятно, влияющим на ремиелинизацию и нейроремонт. Обычно заглушая посредством эпигенетического контроля, некоторые факторы окружающей среды, такие как вирусы (например, вирус Эпштейна-Барр (EBV) и HHV8), приводят к его повторной экспрессии в восприимчивых клетках. Белок ENV присутствует в непосредственной близости от OPCs в нормальном белом веществе (NAWM) в мозге пациентов с MS и способен напрямую вмешиваться в дифференцировку OPC посредством активации Toll-подобного рецептора 4. Клиническое исследование (CHANGE-MS, NCT02782858), в котором приняли участие 270 пациентов, показало значительную пользу GNbAC1 при корковой и таламической атрофии с относительным уменьшением потери объема на 31% и 72% соответственно. Кроме того, количество гипоинтенсивных поражений Т1 (т.е. черных дыр) было снижено на 63% по сравнению с контрольной группой. Кроме того, была полезна MTR как для NAWM, так и для коры головного мозга, что свидетельствует о влиянии на ремиелинизацию.
Окрелизумаб
Окрелизумаб представляет собой моноклональное антитело, направленное против маркера CD20 на поверхности B-клеток, и используется как для первичного прогрессирующего рассеянного склероза (PPMS), так и для RRMS. Хотя было обнаружено, что в RRMS окрелизумаб более эффективен, чем IFN-β-1a, результаты плацебо-контролируемого исследования PPMS следует рассматривать с осторожностью. Первичная конечная точка этого исследования, то есть прогрессирование инвалидности, подтвержденное через 3 месяца, была достигнута только с = 0,03, а относительное снижение риска составило 24%. Исследование, основанное на предыдущем опыте с ритуксимабом, который является другим моноклональным анти-CD20-антителом, предъявлял относительно строгие требования к поступлению, включая возраст от 18 до 55 лет и наличие олигоклональных полос в спинномозговой жидкости (CSF). Это привело к относительно молодой популяции исследования с относительно короткой продолжительностью заболевания и высокой остаточной воспалительной активностью, что подчеркивается тем фактом, что у 24,7% -26,5% пациентов все еще имелись гадолиний-увеличивающие поражения на их базовых МРТ. В результате возможно что влияние окрелизумаба на прогрессирование инвалидности при PPMS в первую очередь опосредовано его противовоспалительными свойствами (как убедительно показано в исследовании RRMS) а не основано на специфических антидегенеративных или нейропротективных механизмах.
Симвастатин
Было показано, что статины, которые широко используются для лечения гиперхолестеринемии, стимулируют дифференцировку OPC. Основываясь на этих и других исследованиях, в исследовании SIMCOMBIN было исследовано, может ли симвастатин быть эффективным в качестве дополнительной терапии IFN-β при RRMS. Используя годовую частоту рецидивов в качестве основной конечной точки, исследование было отрицательным. Тем не менее, во втором исследовании (MS-STAT), включающем 140 пациентов с вторичным прогрессирующим рассеянным склерозом (SPMS), было показано, что симвастатин приводил к значительному снижению среднегодовой атрофии головного мозга на 43%. В настоящее время планируется провести более масштабное исследование MS-STAT2 для привлечения 1180 пациентов с SPMS, чтобы выяснить, может ли симвастатин замедлять прогрессирование SPMS в течение 3-летнего периода (NCT03387670).
Биотин
Биотин является коферментом семейства витаминов группы В, который, как считается, увеличивает выработку миелина за счет увеличения выработки аденозинтрифосфата (АТФ), а также стимулирует синтез жирных кислот. В первом испытании, опубликованном в 2016 году (MS-SPI ) пациенты с прогрессирующим рассеянным склерозом получали биотин ежедневно и подвергались мониторингу для обращения инвалидности, как это определено с помощью снижения показателя по расширенной шкале состояния инвалидности (EDSS) на ± 1 балл (± 0,5 балла для EDSS 6–7) или на снижение на ± 20% по времени 25 Прогулка пешком (TW25). Эта первичная конечная точка была достигнута у 12,6% пациентов, получавших биотин. Во втором исследовании, изучавшем высокие дозы биотина (MS-ON), приняли участие 93 пациента с односторонней или двусторонней оптической невропатией (ON) с постоянной потерей зрения и ухудшением остроты зрения. Здесь, в подгруппе из 31 пациента с прогрессирующим ПО лечение биотином улучшило остроту зрения. Основываясь на результатах исследования SPI, были начаты дальнейшие прогрессивные исследования РС с целью подтверждения предыдущих результатов с большим количеством пациентов и уточненными показаниями (NCT03302806, NCT02936037).
Кветиапина стеарилфумарат
Сообщалось что кветиапин который является атипичным антипсихотическим лекарственным средством в форме соли фумарата, стимулирует дифференцировку нейральных предшественников в олигодендроциты и увеличивает синтез основного белка миелина (MBP). Считается что он увеличивает созревание олигодендроглии и предотвращает токсическую демиелинизацию у мышей C57BL / 6 с помощью купризона. Эти исследования на грызунах побудили провести фазу I исследования, проводимого в настоящее время для определения безопасности и переносимости этого соединения у пациентов с РС (NCT02087631). Примечательно что кветиапина фумарат по химическому составу похож на диметилфумарат, который был одобрен для лечения RRMS в 2013 году. Однако хотя было установлено что диметилфумарат оказывает нейрозащитное действие при нейровоспалительном воздействии с помощью антиоксиданта, связанного с NF-E2-фактором 2 (Nrf2) Таким образом воздействия на ремиелинизацию до сих пор не изучены.
Домперидон
В клинических условиях домперидон, антагонист допаминовых рецепторов D2 / D3, широко используется для лечения тошноты и рвоты. Однако более 30 лет назад было показано, что он увеличивает выработку пролактина у людей. Пролактин стимулирует ремиелинизацию на животных моделях, что побудило начать два этапа II клинических испытаний. Цель первого состоит в том чтобы выяснить может ли домперидон снижать прогрессирование инвалидности в SPMS (NCT02308137), в то время как второе исследует его влияние на RRMS (NCT02493049).
Антисемафорин 4D (VX15 / 2503)
Семафорины, название которых происходит от хорошо известной системы связи на основе флагов ВМС, оказывают плейотропное действие во множестве различных контекстов — от развития до регуляции иммунной системы. Однако они также оказывают непосредственное влияние на миграцию OPC и играют важную роль в активации T-клеток. Один из членов семейства семафоринов, семафорин 4D (Sema4D), активируется в OPC при повреждении спинного мозга, и было обнаружено что он вызывает коллапс расширений процесса в OPC. Блокирование Sema4D привело к сильному снижению воспалительной активности при EAE, что побудило начать фазу I клинического испытания, исследующего безопасность и переносимость гуманизированного моноклонального антитела против Sema4D VX15 / 2503 у пациентов с РС (NCT01764737).
Ремиелинизирующая терапия с доклиническими данными
IRX4204
Было обнаружено что этот специфический агонист гамма-рецепторов ретиноевой кислоты (RXR-γ) стимулирует дифференцировку OPC in vitro и in vivo. В дополнение к своему положительному влиянию на глиогенез, также сообщалось что IRX4204 ингибирует воспаление ЦНС при ЭАЭ. Это вероятно достигается путем изменения баланса Т-клеток, ингибирования потенциально вредных Т-клеток-помощников и стимулирования регуляторной дифференцировки Т-клеток. Таким образом IRX4204 может иметь терапевтическую ценность для лечения MS путем одновременного воздействия на иммунные и нервные клетки. Эта двойная роль в этом контексте в настоящее время исследуется группой ученых в сотрудничестве с Io Therapeutics, Inc. (Санта-Ана, Калифорния).
Каппа опиоидная
Каппа-опиоидный рецептор (KOR) является частью эндогенной опиоидной системы и был идентифицирован как способствующий дифференцировке олигодендроцитов и миелинизации в очищенных олигодендроглиальных совместных культурах. Соединение свинца U-50488 эффективно стимулировало дифференцировку, ускоряло ремиелинизацию in vivo и усиливало дифференцировку OPC, происходящих из плюрипотентных стволовых клеток в зрелые олигодендроциты.
Модуляторы спингозин-1-фосфатных рецепторов
В нашем предыдущем обзоре мы обсуждали эффекты финголимода, модулятора рецептора сфингозин-1-фосфата (S1P), предотвращающего выход лимфоцитов из лимфатических узлов. Однако как известно финголимод также проникает через ГЭБ в мозг где он модулирует поведение популяций резидентных клеток, таких как незрелые олигодендроциты, посредством передачи сигналов RhoA и может усиливать ремиелинизацию. Было обнаружено, что Siponimod, другой модулятор рецептора S1P, особенно нацеленный на рецепторные подтипы S1P1 и S1P5, спасает передачу GABAergic в стриатуме мышей EAE и предотвращает потерю GABAergic интернейронов. Кроме того, это уменьшило астроглиоз и микроглиоз. Изучая его влияние на SPMS, клиническое исследование показало, что сипонимод снижает подтвержденное прогрессирование инвалидности (CDP) на 21%, а также годовой уровень рецидивов (ARR) на 55% за 3 месяца лечения (EXPAND исследование ). Это может отражать тот факт, что, хотя пациенты должны были быть свободными от рецидивов в течение 6 месяцев до включения, приблизительно у 25% все еще имелись гадолиний-повышающие (Gd +) Т1-поражения в начале исследования, что свидетельствует о воспалительной активности. Более того, ни один пациент с ППРС не был зачислен, что приводит к вопросу о том, можно ли эффективно направить нейродегенерацию без какого-либо остаточного воспаления.
Ингибитор γ-секретазы кверцетин
Несколько молекулярных сигнальных каскадов работают параллельно, чтобы ингибировать дифференцировку OPC и ремиелинизацию очагов РС. Например, ингибирование сигнализации олигодендроглиальным Notch через гамма-секретазы уже было показано что может значительно улучшить клиническое выздоровление и ремиелинизацию в EAE. Помимо пути Notch, было также показано что передача сигналов Wnt влияет на (ре) миелинизацию путем ядерной транслокации β-катенина, процесс называемый канонической передачей сигналов Wnt. В ядре β-катенин связывается с фактором транскрипции 4 (Tcf4), который, в свою очередь, задерживает восстановление миелина. Тем не менее существует важное предостережение о том что неизбирательное ингибирование Wnt может мешать как канонической, так и неканонической передаче сигналов Wnt, которая регулирует множество различных клеточных функций. Возможно наиболее перспективным агентом, доступным в настоящее время для селективного ингибирования канонической передачи сигналов Wnt, является флавоноид кверцетин, который уже был исследован при раке толстой кишки и который, как было обнаружено сильно подавляет связывание комплексов Tcf со специфическими сайтами связывания ДНК и нарушить связывание β-катенина с Tcf-4. Кверцетин может поэтому обеспечить фармакологический подход для высокоселективного терапевтического ингибирования передачи сигналов Wnt.
Терифлуномид
Терифлуномид, пероральное лечение первой линии RRMS в Соединенных Штатах и Европейском Союзе (ЕС), является активным метаболитом противоревматического препарата лефлуномид. Предполагается что его иммуномодулирующее действие главным образом основано на ингибировании синтеза пиримидина de novo оказывающего цитостатическое действие на пролиферирующие лимфоциты. Было обнаружено что кратковременная стимуляция терифлуномидом значительно стимулирует олигодендроглиальную дифференцировку включая прямое воздействие на основные факторы транскрипции миелина а также на компоненты челночного белка в ядре. Кроме того, обработка терифлуномидом также привела к образованию зрелых олигодендроцитов, которые эффективно миелинизируют аксоны in vitro. Еще неизвестно может ли он также стимулировать ремиелинизацию in vivo. Если это так это может дать функциональное объяснение наблюдаемому снижению прогрессирования инвалидности в клинических испытаниях (TEMSO, NCT00134563 и TOWER, NCT00751881).
Ремиелинизация: реальный взгляд
Несмотря на значительный прогресс достигнутый с момента первого введения ИФН в начале 1990-х годов, до сих пор не существует эффективного лечения дегенеративных аспектов РС. Прекращение постоянного ухудшения и улучшения приобретенного дефицита остаются неотложными неудовлетворенными клиническими потребностями. К счастью исследовательский конвейер направленный на ремиелинизацию и восстановление содержит несколько агентов, которые показали себя многообещающими как в начальных испытаниях так и на животных моделях. Одним из приоритетов исследований РС является необходимость разработки методов которые могут эффективно измерять эффективность восстановления / ремиелинизации в условиях клинических испытаний. Кроме того при разработке таких методов лечения мы всегда должны учитывать, что безопасность лекарств играет все возрастающую роль как к сожалению показано на примере даклизумаба.
Перевод источник











Алекс, спасибо за подбор статьи. Было бы круто, если бы вы указали отдельно и понятно, что это перевод и источник оригинала. И проработали бы сноски полноценно, а непереадресовывали бы их на оригинальную статью.
Потому что в том виде, в котором статья представлена сейчас — это плагиат.